Contexte clinique
Toxoplasmose
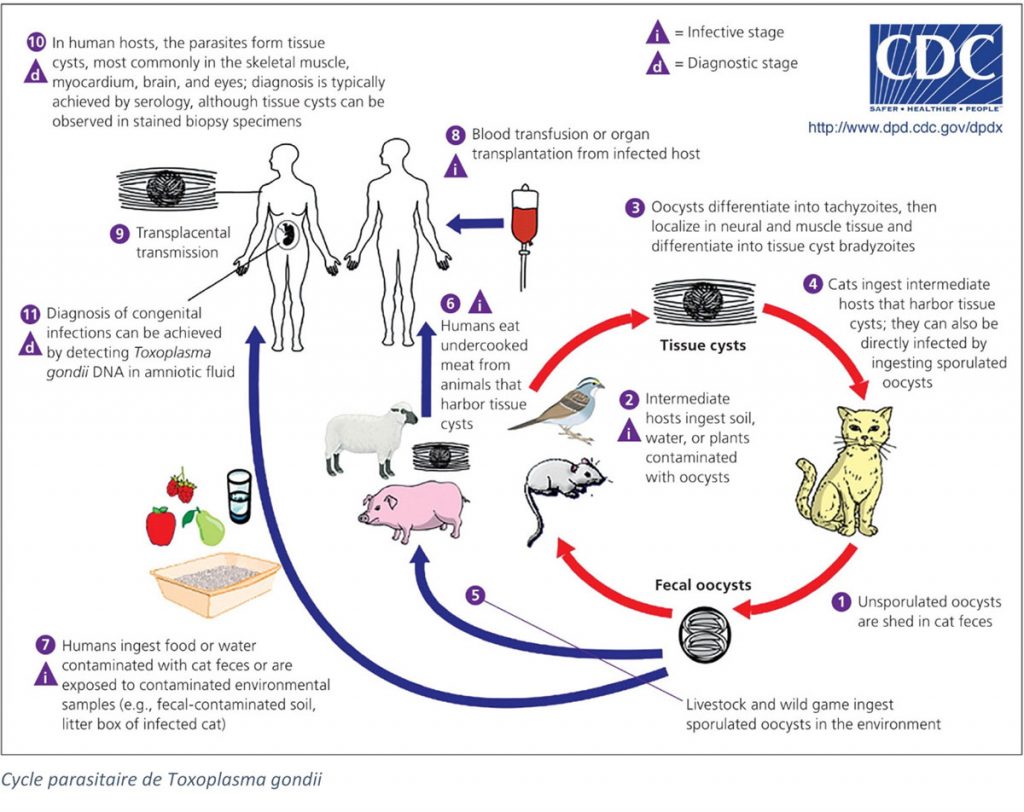 La toxoplasmose est une zoonose causée par le parasite Toxoplasma gondii. Ce protozoaire intracellulaire obligatoire possède un cycle complexe, impliquant plusieurs stades :
La toxoplasmose est une zoonose causée par le parasite Toxoplasma gondii. Ce protozoaire intracellulaire obligatoire possède un cycle complexe, impliquant plusieurs stades :
- Un cycle sexué chez les félins, hôtes définitifs. Le parasite se reproduit lors du stade mérozoïte chez le chat, qui relargue ensuite dans ses déjections la forme oocyste du parasite : c’est le stade sporozoïte.
- Un cycle asexué chez les hôtes intermédiaires, mammifères incluant l’Homme, et les oiseaux. Le parasite prolifère dans des vacuoles chez l’hôte durant le stade tachyzoïte, avant d’infecter n’importe quel type de cellule nucléée, où il sera contenu dans des kystes par plusieurs milliers : stade bradyzoïte.
Si T. gondii est très certainement originaire d’Amazonie (Reiling et al., 2019), la toxoplasmose est la plus fréquente des parasitoses au monde, avec environ 30% de la population mondiale infectée. Cette moyenne cache des disparités régionales importantes (Pappas et al., 2009). La prévalence est en diminution ces dernières années, en particulier dans les pays occidentaux, probablement en raison de l’amélioration des conditions d’hygiènes (Guigue et al., 2018).
L’Homme s’infecte par ingestion de kystes contenus dans la viande crue ou mal cuite, ou d’oocystes présents dans l’eau ou sur des aliments souillés par les déjections de chats infectés. L’infection peut également survenir lors de transplantation d’organes/sang puisque les tachyzoïtes peuvent infecter n’importe quel tissu. La toxoplasmose peut également se transmettre chez le fœtus, on parle alors de toxoplasmose congénitale qui peut être mortelle pour le fœtus ou lui causer des lésions irréversibles (Saadatnia et al., 2012).
Différentes autres expressions cliniques de la toxoplasmose existent en fonction du contexte clinique, du statut immunitaire du patient et de la souche de parasite en cause. Les principaux tableaux cliniques sont celui de la primo-infection, de la toxoplasmose oculaire ou encore de la toxoplasmose de l’immunodéprimé.
Primo-infection
L’infection chez les personnes immunocompétentes est asymptomatique dans la très grande majorité des cas, même chez la femme enceinte. Dans 10% des cas, quelques symptômes non spécifiques sont observés, sans demander de traitement particulier. Toutefois, des formes cliniques plus graves (fièvres, céphalées, asthénie, vomissements importants, atteintes oculaires ou plus rarement pulmonaire) peuvent être observées chez l’immunocompétent en particulier dans le cas d’une infection par certaines souches très virulentes, la plupart étant retrouvées en Amérique latine (Dubey et al., 2012).
Chez les patients immunocompétents, en raison du caractère le plus souvent asymptomatique de l’infection et de la non-spécificité des symptômes (tableau clinique proche des infections à CMV, EBV ou primo-infection VIH), le diagnostic repose sur la sérologie. Comme la présence d’IgG seule ne permet pas d’écarter le diagnostic d’une infection ancienne, le diagnostic de primo-infection s’appuie sur plusieurs tests pour essayer de dater l’infection. En cas de forme clinique, une recherche de toxoplasme par PCR peut être une technique envisageable.
La détermination d’une primo-infection peut être aisée en cas de connaissance de l’antériorité sérologique de la patiente, ou plus complexe en cas de premier prélèvement positif en cours de grossesse. Dans ce cas, plusieurs indicateurs, tous imparfaits, peuvent être utilisés : la présence d’IgM, l’avidité des IgG, la présence d’IgA (Olariu et al., 2019), l’évolution du titre des anticorps (Montoya et al.,2008). La présence d’IgM, telle que détectée en ELISA le plus souvent est théoriquement un marqueur de primo-infection mais elle manque de spécificité (Villard et al., 2016a) et des IgM résiduelles sont détectées dans un nombre important de cas : 1 an après l’infection entre 9 et 27% des patients auraient encore des IgM détectables (Villard et al., 2016b). L’avidité des IgG permet également une datation et d’exclure une infection récente en cas d’avidité forte. Cependant, certains patients ne développent jamais d’avidité forte et une avidité faible ne permet pas de conclure à une infection récente. Enfin, une hausse importante des taux d’IgG entre 2 prélèvements espacés de deux semaines est en faveur d’une infection récente. A l’inverse, des taux d’IgG stables indiquent une infection vieille de plus de 3 mois (Villard et al., 2016b).
En raison du caractère le plus souvent asymptomatique de l’infection, et des difficultés de datation de l’infection, le suivi systématique des femmes enceintes pendant la grossesse, bien que non réalisé dans tous les pays, est un puissant moyen de prévention de la toxoplasmose congénitale. Par exemple, en France, le statut immunologique des femmes enceintes est établi dans le premier trimestre de la grossesse. En cas de test négatif, une sérologie mensuelle est mise en place. Pour les cas de séroconversion ou de suspicion d’infection récente, une recherche de toxoplasmose congénitale doit être mise en place. Le suivi prénatal de la toxoplasmose est considéré comme une technique bénéfique en termes de santé publique : le rapport cout-bénéfice est très en faveur de cette approche (Prusa et al., 2017), tout comme le rapport coût-efficacité (Binquet et al., 2019).
Il existe de nombreuses techniques sérologiques (immunofluorescence indirecte, ELISA, ISAGA), mais la plus répandue reste l’ELISA, avec des techniques spécifiques des IgM et des IgG isolées. Ces techniques ont des performances variables et demandent un suivi précis de la cinétique immunologique propre à chaque patient, d’autant plus que les titres d’anticorps habituellement mesurés sont très faibles, avec des zones grises parfois importantes (Villard et al., 2016a, Robert-Gangneux et al., 2012).
Pour réaliser un diagnostic initial ou pour le suivi des femmes enceintes, nous avons développé un test rapide et robuste, le test Toxoplasma ICT IgG-IgM. Particulièrement adapté aux laboratoires de première ligne ou aux laboratoires réalisant de petites séries, il remplace de manière avantageuse les autres techniques de dépistage.
En cas de résultats équivoques ou discordants entre les techniques de dépistage, la Haute Autorité de Santé en France recommande un test de confirmation par immunoblot ou dye-test, cette dernière technique, laborieuse et non standardisée, étant réservée à des centres de référence (Argumentaire HAS, 2017a).
Pour pouvoir répondre à l’exigence de la demande, nous avons développé un test fiable basé sur la technique de Western Blot. Couplé à l’utilisation d’antigènes naturels (T. gondii) hautement sensibles et spécifiques, les tests LDBIO Toxo II IgG et LDBIO Toxo II IgM se positionnent ainsi parfaitement en tant que test de confirmation de la sérologie IgG ou IgM, y compris en cas de très faible taux sérologique.
Toxoplasmose oculaire
La toxoplasmose oculaire survient souvent dans un contexte de toxoplasmose congénitale. Cependant, en particulier en cas d’infection par une souche virulente comme celles retrouvées en Amérique du Sud, des toxoplasmoses oculaires sont aussi retrouvées lors de la phase aigüe de l’infection aussi bien que lors d’une réactivation, causant des lésions de la rétine en association avec une forte réaction inflammatoire. En fonction de la localisation, la toxoplasmose oculaire peut impacter la vision voire entraîner une perte définitive de la vision d’un ou des deux yeux (Butler et al., 2013).
L’approche diagnostique de la toxoplasmose oculaire est très spécifique et se rapproche de celle d’une toxoplasmose congénitale, dont elle est une des manifestations. Elle est donc détaillée dans la section toxoplasmose congénitale.
Toxoplasmose de l’immunodéprimé
Chez les personnes immunodéprimées, la toxoplasmose peut être beaucoup plus sévère. En fonction de la cause et de l’intensité de l’immunodépression, plusieurs tableaux différents peuvent être retrouvés :
- Primo-infection ou réactivation toxoplasmique chez un sidéen en phase SIDA avancée (CD4<100). Dans ce cas-là, l’atteinte est le plus souvent cérébrale, sous forme d’encéphalites (Vidal, 2019). La toxoplasmose est l’une des principales causes de décès des patients en phase de SIDA. De plus, la HAS en France recommande un suivi régulier des patients VIH négatifs en toxoplasmose (Argumentaire HAS, 2017b). Pour les patients positifs en toxoplasmose, et avec les CD4 fortement diminués (<100/mm3), une prophylaxie anti-Pneumocystis, également active sur Toxoplasma devrait être proposée.
- Receveurs positifs ou missmatch donneur positif / receveur négatif dans un contexte de greffe d’organe solide, en particulier cardiaque ou de greffe de moelle. Dans ces cas-là, le risque est celui d’une infection aiguë en raison de l’immunodépression engendrée par le traitement. C’est pourquoi le Centre National de Référence pour la toxoplasmose en France recommande une analyse sérologique de la toxoplasmose avant la greffe (Villard et al., 2016a). Le risque est majoré pour les greffes de moelle et les transplantations cardiaques (en cas de donneur positif et en raison d’un tropisme cardiaque du parasite). En cas de receveur positif ou de missmatch, un traitement prophylactique doit être mis en place (Dard et al., 2018).
En raison de la faiblesse humorale de la réponse des patients immunodéprimés, il est fréquent d’obtenir des sérologies faussement négatives ou non interprétables. La PCR sur sang périphérique est alors l’examen diagnostic préférentiel (Villard et al., 2016a). Toutefois, en particulier en cas d’absence d’antécédents sérologiques pour un patient immunodéprimé, et afin d’éviter le risque de résultat faussement négatif, certains auteurs préconisent d’abaisser les seuils de recontrôle des techniques de screening dans cette population puis de confirmer avec une technique de confirmation (Douet et al., 2020).
Pour pouvoir répondre à l’exigence de la demande, nous avons développé un test fiable basé sur la technique de Western Blot. Couplé à l’utilisation d’antigènes naturels (T. gondii) hautement sensibles, le test LDBIO Toxo II IgG se positionne ainsi parfaitement en tant que test de confirmation du diagnostic de la toxoplasmose, y compris en cas de très faible taux sérologique.
RÉFÉRENCES SCIENTIFIQUES
- Begeman IJ, Lykins J, Zhou Y, Lai BS, Levigne P, El Bissati K, et al. Point-of-care testing for Toxoplasma gondii IgG/IgM using Toxoplasma ICT IgG-IgM test with sera from the United States and implications for developing countries. 2017; PLoS Negl Trop Dis 11(6): e0005670.
- Douet T, Armengol C, Charpentier E, Chauvin P, Cassaing S, Iriart X, et al. Performance of seven commercial automated assays for the detection of low levels of anti-Toxoplasma IgG in French immunocompromised patients. 2019; Parasite. 26:51.
- Franck J, Garin YJ, Dumon H. LDBio-Toxo II immunoglobulin G Western blot confirmatory test for anti-toxoplasma antibody detection. 2008; J Clin Microbiol.
- Jost C, Touafek F, Fekkar A, Courtin R, Ribeiro M, Mazier D, et al. Utility of immunoblotting for early diagnosis of toxoplasmosis seroconversion in pregnant women. 2011; Clin Vaccine Immunol. 18(11):1908-1912.
- Lykins J, Li X, Levigne P, Zhou Y, El Bissati K, Clouser F, et al. Rapid, inexpensive, fingerstick, whole-blood, sensitive, specific, point-of-care test for anti-Toxoplasma antibodies. 2018; PLoS Negl Trop Dis 12(8): e0006536.
- Mahinc C, Flori P, Delaunay E, Guillerme C, Charaoui S, Raberin H, et al. Evaluation of a new immunochromatography technology test (LDBio Diagnostics) to detect Toxoplasma IgG and IgM: comparison with the routine Architect technique. 2017; J Clin Microbiol 55:3395–3404.
- Maudry A, Chene G, Chatelain R, Patural H, Bellete B, Tisseur B, et al. Bicentric evaluation of six anti-toxoplasma immunoglobulin G (IgG) automated immunoassays and comparison to the Toxo II IgG Western blot. 2009; Clin Vaccine Immunol. 16(9):1322-1326.
- Villard O, Cimon B, L’Ollivier C, Fricker-Hidalgo H, Godineau N, Houze S, et al. Help in the Choice of Automated or Semiautomated Immunoassays for Serological Diagnosis of Toxoplasmosis: Evaluation of Nine Immunoassays by the French National Reference Center for Toxoplasmosis. 2016a; J Clin Microbiol. 54(12):3034-3042.
- Villard O, Cimon B, L’Ollivier C, Fricker-Hidalgo H, Godineau N, Houze S, et al. et al. Serological diagnosis of Toxoplasma gondii infection: Recommendations from the French National Reference Center for Toxoplasmosis. Diagn Microbiol Infect Dis. 2016b;84(1):22-33.
Nos produits
Commander
Pour commander en France, écrivez-nous à notre adresse Order en indiquant les références et descriptions des produits que vous souhaitez, ou téléphonez au 04 78 83 34 87.
